Drugi dzień na Forum Rynku Zdrowia rozpoczęliśmy od debaty na temat innowacyjnych technologii medycznych. O różnicy pomiędzy innowacją a nowością w obszarze wyrobów medycznych oraz o tym, jak wygląda ścieżka dostępu do nich dla pacjentów, mówiła w naszym imieniu Sylwia Piekarska.
Przewodnicząca sekcji ds. wyrobów medycznych stosowanych w procedurach szpitalnych reprezentowała nas podczas panelu: Innowacje w sektorze medycznym.
Prelegenci:
- Dominik Dziurda (dyrektor, Wydział Świadczeń Opieki Zdrowotnej, Agencja Oceny Technologii Medycznych i Taryfikacji)
- Krzysztof Górski (dyrektor, Wydział Nauki i Finansowania Projektów, Agencja Badań Medycznych)
- Krzysztof Kurek (członek zarządu ds. medycznych, Grupa LUX MED)
- Anna Mirek (radca prawny, senior associate, Kancelaria Noerr)
- Sylwia Piekarska (przewodnicząca sekcji ds. wyrobów szpitalnych w procedurach szpitalnych, Izba POLMED)
- Adam Szabuniewicz (dyrektor sprzedaży, Comarch Healthcare SA)
- Piotr Węcławik (dyrektor, departament innowacji, Ministerstwo Zdrowia)
Moderator dyskusji: Ligia Kornowska (Koalicja AI w Zdrowiu, dyrektor zarządzająca, Polska Federacja Szpitali)
Jak wygląda procedura wdrażania nowych technologii w naszym kraju?
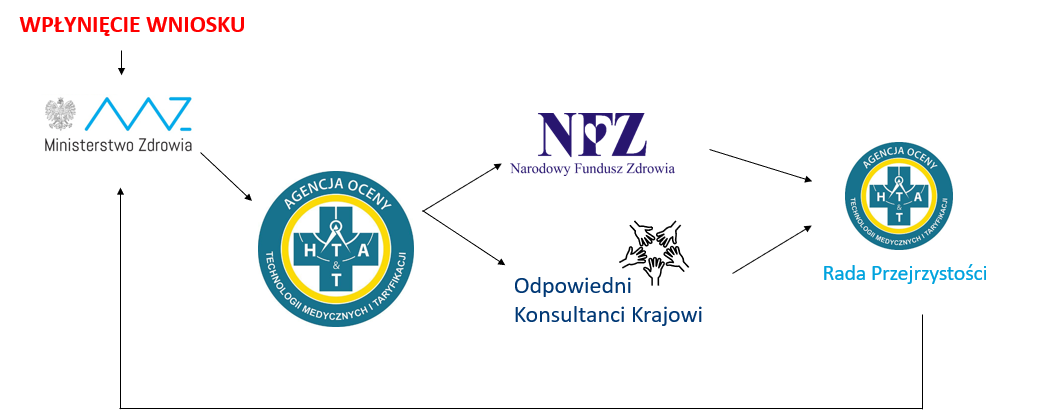
Aktualna procedura wdrażania nowych technologii do koszyka świadczeń gwarantowanych jest opisana w ustawie o świadczeniach opieki zdrowotnej finansowanych ze środków publicznych w rozdziale 1a. Można ją zaprezentować prostym schematem:
Zgodnie z art. 31c Minister Zdrowia zleca Prezesowi AOTMiT przygotowanie rekomendacji dla danego świadczenia opieki zdrowotnej w sprawie jego zakwalifikowania jako świadczenia gwarantowanego. AOTMiT konsultuje to następnie z NFZ oraz właściwymi konsultantami krajowymi, przedstawia Radzie Przejrzystości i na końcu wydaje rekomendację Ministrowi Zdrowia. Brak jest określenia zarówno terminu w jakim należy taką rekomendację przygotować, jak i trybu selekcji świadczeń, w sprawie których występuje Minister Zdrowia. Skutkuje to niezwykle długotrwałym procesem wydawania rekomendacji, tak że wydanie rekomendacji dla „innowacyjnego” świadczenia następuje niekiedy w momencie, w którym przestaje być ono już stosowane (innowacyjne).
Czy nadużywamy słowa „innowacja”?
 “W obszarze wyrobów i technologii medycznych nieraz mylimy innowację z nowością. A przecież nie każda nowa procedura czy świadczenie, które pojawiają się w koszyku świadczeń gwarantowanych to rozwiązania innowacyjne; najczęściej gonimy światowy standard opieki i z opóźnieniem wprowadzamy w Polsce te rozwiązania. Nowość w Polsce to często już od wielu lat standard opieki w innych krajach.” – mówiła Sylwia Piekarska.
“W obszarze wyrobów i technologii medycznych nieraz mylimy innowację z nowością. A przecież nie każda nowa procedura czy świadczenie, które pojawiają się w koszyku świadczeń gwarantowanych to rozwiązania innowacyjne; najczęściej gonimy światowy standard opieki i z opóźnieniem wprowadzamy w Polsce te rozwiązania. Nowość w Polsce to często już od wielu lat standard opieki w innych krajach.” – mówiła Sylwia Piekarska.
“Finansowanie wyrobów i technologii medycznych – w tym innowacyjnych – musi być przede wszystkim transparentne i uzasadnione. Dobrze, by ścieżka wprowadzania nowych rozwiązań do systemu odpowiadała dynamice rozwoju branży. Izba POLMED postuluje też o nadanie prawa do wnioskowania o refundację producentom i dystrybutorom wyrobów/technologii medycznych.” – dodała S. Piekarska
Dziękujemy portalowi RynekZdrowia.pl za zaporszenie Izby POLMED do panelu, a wszystkim prelegentom za udział w tej ciekawej i merytorycznej dyskusji.